Ám ảnh với mRNA
Katalin Kariko lớn lên ở Hungary và là con gái của một người bán thịt. Dù chưa bao giờ được tiếp xúc với một nhà khoa học nào, nhưng từ nhỏ, Katalin Kariko đã ấp ủ ước mơ trở thành một người nghiên cứu. Bà chuyển đến Mỹ ở độ tuổi 20. Song, suốt nhiều thập kỷ, Kariko không thể tìm được một vị trí lâu dài.
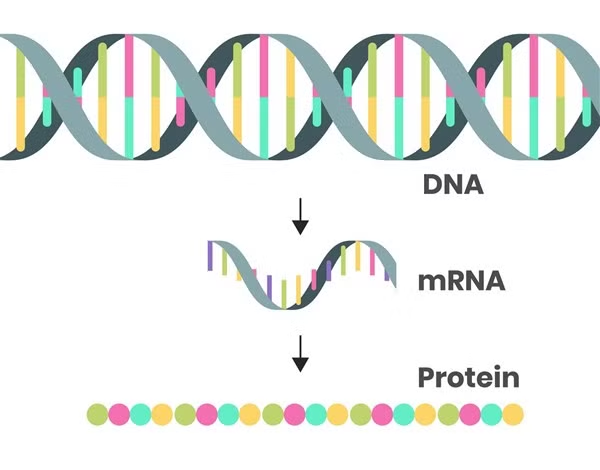
Trong suốt sự nghiệp của mình, Tiến sĩ Kariko đã tập trung vào mRNA. Đây là vật liệu di truyền mang các chỉ dẫn ADN đến bộ máy tạo ra protein của mỗi tế bào. Bà Kariko tin rằng, mRNA có thể được sử dụng để sản xuất thuốc, bao gồm cả vắc-xin chống lại Covid-19.
Song, trong nhiều năm, sự nghiệp của nhà khoa học này tại Đại học Pennsylvania không hề thuận lợi. Bà chuyển từ phòng thí nghiệm này sang phòng thí nghiệm khác. Thậm chí, Kariko chưa bao giờ kiếm được hơn 60.000 USD/năm.
Tiến sĩ Anthony Fauci - Giám đốc Viện Quốc gia về Dị ứng và Bệnh truyền nhiễm Quốc gia Mỹ, chia sẻ: “Theo nghĩa tích cực, Kariko bị ám ảnh bởi khái niệm RNA thông tin”.
Tiến sĩ Kariko thường xuyên đấu tranh để có thể tiếp tục trụ vững trong học viện. Bà cần tài trợ để theo đuổi những ý tưởng có vẻ hoang đường và viển vông. Tiến sĩ David Langer - một nhà giải phẫu thần kinh từng làm việc với Tiến sĩ Kariko cho biết: “Khi ý tưởng của bạn đi ngược lại với sự khôn ngoan thông thường, nó rất khó đột phá”.
Ý tưởng của Tiến sĩ Kariko về mRNA chắc chắn là ví dụ điển hình của câu nói này.
Đối với Tiến sĩ Kariko, hầu hết thời gian trôi qua đều là trong phòng thí nghiệm. Với nhiều nhà khoa học, theo sau một khám phá mới là kế hoạch kiếm tiền, thành lập công ty và nhận bằng sáng chế. Song, Tiến sĩ Kariko không có khái niệm đó.
“Đó là điều xa vời nhất trong tâm trí Kate”, Tiến sĩ Langer nói.
Nhiều lần thất bại

Tiến sĩ Kariko Katalin.
Kariko lớn lên ở thị trấn nhỏ Kisujszallas của Hungary. Bà lấy bằng Tiến sĩ tại Đại học Szeged và làm nghiên cứu sinh sau tiến sĩ tại Trung tâm Nghiên cứu Sinh học.
Năm 1985, khi chương trình nghiên cứu của trường đại học hết kinh phí, Tiến sĩ Kariko cùng chồng và con gái 2 tuổi - Susan, chuyển đến Philadelphia (Mỹ).
Khi đó, tài sản duy nhất có giá trị của họ là chiếc ô tô cũ, bán được 900 bảng Anh ở chợ đen. Để mang trót lọt số tiền ấy sang Mỹ, Kariko Katalin phải rạch gấu bông đồ chơi của con gái, nhét 900 bảng vào, rồi khâu lại. Bà tiếp tục làm nghiên cứu sinh sau tiến sĩ tại Đại học Temple (Mỹ).
Những ngày đầu bước vào lĩnh vực mRNA, ngay cả những nhiệm vụ cơ bản nhất cũng vô cùng khó khăn, nếu không muốn nói là không thể. Làm thế nào để tạo ra các phân tử RNA trong phòng thí nghiệm? Làm thế nào để đưa mRNA vào các tế bào của cơ thể?
Năm 1989, bà Kariko và Tiến sĩ Elliot Barnathan, khi đó là bác sĩ tim mạch tại Đại học Pennsylvania, lên kế hoạch đưa mRNA vào các tế bào. Từ đó, khiến chúng tạo ra các protein mới. Ở một trong những thí nghiệm đầu tiên, họ hy vọng sử dụng chiến lược này để hướng dẫn các tế bào tạo ra một loại protein được gọi là thụ thể urokinase.
“Hầu hết, mọi người đều cười nhạo chúng tôi”, Tiến sĩ Barnathan hồi tưởng. Sau quá trình nghiên cứu, họ phát hiện, mRNA có thể được sử dụng để chỉ đạo bất kỳ tế bào nào tạo ra protein theo ý muốn.
“Tôi cảm thấy mình như một vị thần”, Tiến sĩ Kariko nhớ lại.
Bà Kariko và Tiến sĩ Barnathan nảy ra nhiều ý tưởng, như sử dụng mRNA để cải thiện mạch máu. Thậm chí là sử dụng quy trình này để kéo dài tuổi thọ của tế bào người.
Tuy nhiên, Tiến sĩ Barnathan đã sớm rời Trường Đại học Pennsylvania, nhận vị trí khác tại một công ty công nghệ sinh học. Thời điểm đó, Tiến sĩ Kariko không có phòng thí nghiệm hay hỗ trợ tài chính. Mặc dù là giáo sư chính thức, nhưng đây là thời gian khó khăn nhất, lương rất thấp và không ai tin bà.
Thời điểm đó, Tiến sĩ Langer hy vọng có thể sử dụng mRNA để điều trị cho những bệnh nhân có máu đông sau phẫu thuật não, thường dẫn đến đột quỵ. Ý tưởng là làm cho các tế bào trong mạch máu tạo ra oxit nitric. Đây là chất làm giãn nở mạch máu, nhưng có thời gian bán hủy là mili giây.
Ông và Tiến sĩ Kariko đã thử mRNA trên các mạch máu cô lập được sử dụng để nghiên cứu đột quỵ. Song, nghiên cứu đã thất bại. Họ tiếp tục đi bộ qua tuyết ở Buffalo, N.Y., để thử trong phòng thí nghiệm trên những con thỏ dễ bị đột quỵ. Thất bại một lần nữa xảy đến.
Sau đó, Tiến sĩ Langer cũng rời trường đại học. Tiến sĩ Kariko tiếp tục rơi vào tình trạng không có phòng thí nghiệm và kinh phí để nghiên cứu. Mọi thứ trở nên tội tệ hơn vào năm 1995, Kariko không nhận được tài trợ, không tìm nổi dự án và Đại học Pennsylvania quyết định sa thải bà.
Thành công đến muộn

Gia đình Tiến sĩ Kariko Katalin.
Vào năm 1998, Kariko Katalin cuối cùng đã nhận được khoản tiền tài trợ 100.000 USD đầu tiên. Thật kì lạ, năm đó bà cũng gặp được một người đàn ông của cuộc đời. Đó là buổi chiều định mệnh, Kariko Katalin đi photo tài liệu, bà gặp Drew Weissmen - một người đồng nghiệp vừa chuyển đến từ Viện Y tế Quốc gia.
Trong lúc chờ, Kariko Katalin kể với Weissmen về ý tưởng tạo ra mRNA. Ngay lập tức, Weissmen nhìn thấy trước mắt mình là một khối tài sản vô giá. Weissmen quyết định đầu tư, cộng tác cùng Kariko Katalin, quyết tâm phát triển công nghệ mRNA trong lĩnh vực y sinh học.
“Tôi đã nói, tôi là một nhà khoa học RNA. Tôi có thể tạo ra bất cứ thứ gì với mRNA”, Tiến sĩ Kariko nhớ lại.
Khi đó, Tiến sĩ Weissman cho biết, ông muốn tạo ra một loại vắc-xin chống lại H.I.V. “Tôi đã nói, Vâng, vâng, tôi có thể làm được”, Tiến sĩ Kariko chia sẻ. Bất chấp sự can đảm này, nghiên cứu về mRNA của Tiến sĩ Kariko không suôn sẻ.
Nhà khoa học này có thể tạo ra các phân tử mRNA hướng dẫn các tế bào trong đĩa petri tạo ra loại protein được chọn. Song, mRNA không hoạt động ở chuột sống.
“Không ai biết tại sao. Tất cả những gì chúng tôi biết là chuột bị bệnh. Bộ lông của chúng bị xù lên, chúng bỏ ăn, bỏ chạy”, Tiến sĩ Weissman nói.
Điều này chứng tỏ, hệ thống miễn dịch nhận ra vi khuẩn xâm nhập bằng cách phát hiện mRNA và phản ứng với tình trạng viêm. Việc tiêm mRNA vào hệ thống miễn dịch giống như một cuộc xâm lược của mầm bệnh.
Thực tế, mỗi tế bào trong cơ thể con người đều tạo ra mRNA và hệ thống miễn dịch “ngó lơ” điều đó. “Tại sao mRNA tôi tạo ra lại khác?”, Tiến sĩ Kariko tự hỏi.
Một đối chứng trong thử nghiệm cuối cùng đã cung cấp manh mối. Tiến sĩ Kariko và Tiến sĩ Weissman nhận thấy, mRNA do họ tạo ra gây phản ứng quá mức miễn dịch. Tuy nhiên, các phân tử điều khiển - một dạng RNA khác trong cơ thể con người, còn được là RNA vận chuyển, hoặc tRNA - thì không.
Một phân tử được gọi là pseudouridine trong tRNA cho phép nó tránh được phản ứng miễn dịch. Hóa ra, mRNA tự nhiên của con người cũng chứa phân tử.
Được thêm vào mRNA do Tiến sĩ Kariko và Tiến sĩ Weissman tạo ra, phân tử này cũng hoạt động tương tự và khiến mRNA mạnh hơn nhiều. Kết quả là, mRNA chỉ đạo tổng hợp lượng protein nhiều gấp 10 lần trong mỗi tế bào. Điều đó có nghĩa là mRNA có thể được sử dụng để thay đổi các chức năng của tế bào mà không gây ra sự tấn công của hệ thống miễn dịch.
Tuy nhiên, cả hai nhà khoa học đã gặp nhiều khó khăn khi kêu gọi tài trợ. Thời gian đầu, hầu hết mọi người đều không hứng thú với mRNA. Những người được kêu gọi tài trợ cho biết, mRNA sẽ không phải là một liệu pháp tốt.
Các tạp chí khoa học hàng đầu cũng từ chối công trình của họ. Khi nghiên cứu được công bố trên tạp chí Immunity, hầu như không mấy ai chú ý đến phát hiện mới.
Vào năm 2005, mRNA phiên bản mô-đun suy yếu ra đời. Sau khi đọc công trình nghiên cứu, Derrick Rossi, một chuyên gia tế bào gốc Canada đang làm nghiên cứu sinh tại Đại học Stanford đã vô cùng kinh ngạc.
Thời cơ đã đến. Nhận thấy cơ hội kinh doanh siêu lợi nhuận, Rossi âm thầm lặng lẽ tìm vốn đầu tư, ông thành lập một công ty bé nhỏ, lấy tên là Moderna.
Tại Đức, một nhóm nghiên cứu mới cũng phát hiện ra tiềm năng của Kariko Katalin, công ty mới BioNTech được thành lập, lấy trụ sở tại Mỹ. Năm 2013, BioNTech thuê Karko Katalin làm chuyên gia cao cấp mRNA.
Người hùng cứu thế giới
Ngay sau đó, các thử nghiệm lâm sàng về vắc-xin cúm mRNA đã được tiến hành. Các nhà khoa học đã nỗ lực chế tạo vắc-xin mới chống lại cytomegalovirus và virus Zika, cùng những virus khác. Sau đó là Coronavirus.
Tháng 1/2020, các nhà khoa học Trung Quốc công bố trình tự di truyền của SARS-CoV-2. BioNTech đã thiết kế vắc-xin mRNA trong vài giờ. Trong khi đó, Moderna thiết kế trong hai ngày.
Ý tưởng cho cả hai loại vắc-xin là đưa mRNA vào cơ thể để hướng dẫn các tế bào của con người sản xuất protein tăng đột biến của Coronavirus. Hệ thống miễn dịch sẽ nhìn thấy protein, nhận ra và học cách tấn công, nếu virus xuất hiện trong cơ thể.
Vào ngày 8/11, kết quả đầu tiên của nghiên cứu Pfizer-BioNTech đã được đưa ra, cho thấy vắc-xin mRNA cung cấp khả năng miễn dịch mạnh mẽ đối với loại virus mới. Tiến sĩ Kariko đã cảm thán với chồng: “Ồ, nó hoạt động. Em nghĩ vậy”.
Để ăn mừng, nữ tiến sĩ đã ăn... một hộp đậu phộng phủ socola Goobers.
Trong khi đó, Tiến sĩ Weissman chia sẻ: “Ước mơ của tôi luôn là phát triển một thứ gì đó trong phòng thí nghiệm để giúp ích cho mọi người. Tôi đã thỏa mãn ước mơ của đời mình”.
Tiến sĩ Kariko và Tiến sĩ Weissman đã được tiêm vắc-xin phòng Covid-19 vào ngày 18/12/2020 tại Đại học Pennsylvania.