Chưa đủ dữ liệu
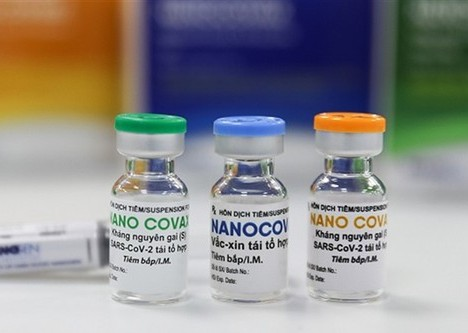
Ngày 18/9, Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia đã họp đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 vắc-xin Nanocovax với kết quả nghiên cứu tính đến ngày 2/9.
Đến nay, vắc-xin Nanocovax đạt yêu cầu về tính an toàn trong ngắn hạn dựa trên dữ liệu báo cáo kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3. Đồng thời, có tính sinh miễn dịch dựa trên dữ liệu báo cáo kết quả giữa kỳ thử nghiệm lâm sàng.
Hiện, chưa có dữ liệu để đánh giá trực tiếp hiệu lực bảo vệ của vắc-xin Nanocovax dựa trên số trường hợp mắc Covid-19 trong nghiên cứu, cần tiếp tục thực hiện đánh giá về hiệu lực bảo vệ theo đề cương được phê duyệt.
Ước tính hiệu quả bảo vệ của vắc-xin Nanocovax dựa trên dữ liệu về tính sinh miễn dịch của vắc-xin nghiên cứu đảm bảo tính khoa học để chuyển hồ sơ tới Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc xem xét.
Hội đồng Đạo đức cho biết, đến nay, vẫn chưa có dữ liệu để đánh giá trực tiếp dựa trên số trường hợp mắc Covid-19 trong nghiên cứu. Đơn vị nghiên cứu cần tiếp tục thực hiện đánh giá về hiệu lực bảo vệ theo đề cương được phê duyệt.
Như vậy, vắc-xin Nanocovax còn một bước xét duyệt nữa để được cấp phép khẩn cấp. Nếu được thông qua, Hội đồng Tư vấn sẽ đề xuất Bộ Y tế cấp phép khẩn cấp cho Nano Covax.
“Tiêu chuẩn vàng” của vắc-xin
PGS.TS Trần Huỳnh - Đại học Y khoa California Northstate (Mỹ) nhận định, việc sản xuất vắc-xin Nanocovax là một bước tiến của ngành y sinh học Việt Nam.
“Hệ miễn dịch chúng ta là một bộ máy phức tạp. Các kháng thể làm việc chặt chẽ với tế bào T cell, B cell, nhiều tế bào APC, và hàng nghìn tế bào miễn dịch khác. Vì vậy, khi chúng ta thấy có kháng thể đặc hiệu trong nghiên cứu vắc-xin, điều đó chưa hẳn là vắc-xin có thể bảo vệ được bệnh”, chuyên gia giải thích.
Theo đó, tiêu chuẩn vàng của vắc-xin phòng Covid-19 là khả năng bảo vệ chống lại bệnh. PGS Huỳnh dẫn chứng, trong các nghiên cứu nhóm đối chứng của Pfizer, Moderna, Astrazeneca, hay Sputnik, thước đo cuối cùng và quan trọng nhất là có bao nhiêu bệnh nhân bị nhiễm bệnh khi tiêm và không tiêm vắc-xin.
“Với vắc-xin Pfizer, thử nghiệm trên 43.448 người ở 2 nhóm đối chứng, có 8 người nhiễm Covid-19 trong số 21.720 người chích vắc-xin. Trong khi đó, có 162 người nhiễm Covid-19 ở 21.728 người không chích vắc-xin”, chuyên gia dẫn chứng.
Ngoài ra, PGS Huỳnh cho biết, một vắc-xin thành công tạo đủ kháng thể, hiệu quả lâm sàng và hiệu quả thực tế. Tạo kháng thể thường là bước đầu tiên thành công trong thử nghiệm vắc-xin.
Sau đó, các nghiên cứu đối chứng lâm sàng chỉ ra hiệu quả lâm sàng là vắc-xin có thể bảo vệ bao nhiêu người không mắc bệnh trong các nhóm. Cuối cùng, khi tiêm vắc-xin ra ngoài thực tế, hiệu quả chỉ ra vắc-xin có thể bảo vệ bao nhiêu người khỏi mắc bệnh.
“Các công bố gần đây nhất của vắc-xin Nanocovax chưa thấy các dữ liệu về ca nhiễm và không nhiễm bệnh trong các nhóm đối chứng. Đây là dữ liệu quan trọng nhất để có tính hiệu quả bảo vệ của vắc-xin. Không có các dữ liệu này, vẫn chưa nói được gì về hiệu quả thật sự của vắc-xin”, PGS Huỳnh nhận định.
Theo chuyên gia này, biết bao nhiêu người nhiễm hay không nhiễm bệnh sẽ giúp ước tính được hiệu quả lâm sàng của vắc-xin Nanocovax.
“Vắc-xin Nanocovax của Việt Nam chưa có đủ dữ liệu chứng minh hiệu quả lâm sàng trong việc ngừa bệnh Covid-19.
Tôi đồng ý với nhận định của Bộ Y tế Việt Nam là vẫn chưa đủ dữ liệu để rút ra kết luận vắc-xin Nanocovax có hiệu quả bảo vệ bệnh Covid-19 và biến thể Delta”, PGS Trần Huỳnh chia sẻ.