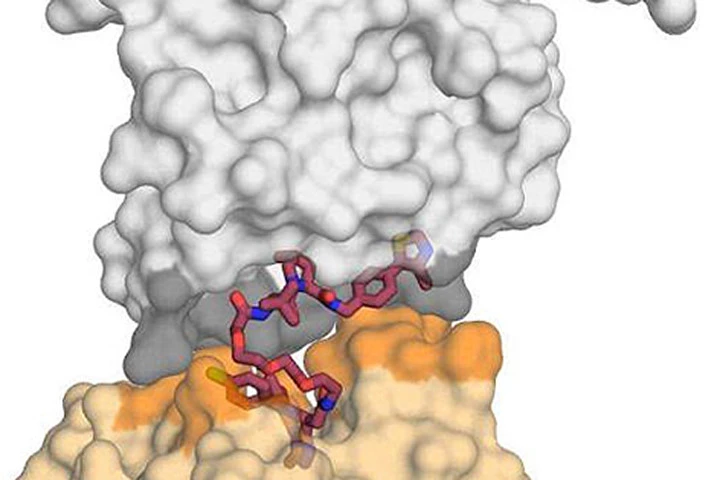
Phương pháp buộc các phân tử liên kết với những khối u hiểm, để lan rộng protein Ras và Myc. Đến thời điểm này, đây là bước đột phá hứa hẹn nhất trong cuộc chiến chống lại căn bệnh ung thư.
Trưởng nhóm nghiên cứu, giáo sư Alessio Ciulli, nói: "Chúng tôi nhận thấy một điều quan trọng là không đủ protein trung hòa để đặt cạnh các protein có hại. Những protein như Ras và Myc phải kết nối trực tiếp với protein có hại hay “hôn” nó. Trong phương pháp này, “nụ hôn thần chết” là chìa khóa để đảm bảo sự suy biến của những protein có hại.”
Ras và Myc được biết là nguyên nhân gây ra ung thư ở người, và Huntingtin - gây ra bệnh Huntingdon (bệnh thoái hóa tiến triển mà nguyên nhân là do tế bào thần kinh trong não mất đi). Tuy nhiên, đến nay chúng vẫn có khả năng kháng lại tất cả các loại thuốc. Hiện tại, một nhóm nghiên cứu do Giáo sư Ciulli thuộc khoa Khoa học Đời sống ở Dundee đã tìm ra cách khắc phục điều này.

Công nghệ mới giúp chữa trị ung thư (Ảnh: Trường đại học Dundee)
Trong lĩnh vực nghiên cứu và điều trị ung thư thì phương pháp này không giống bình thường. Nó sử dụng cách tiếp cận các phân tử nhỏ, nhằm mục tiêu vào các protein gây hại bằng cách gắn nó với các chất trung hòa. Từ đó bắt đầu quá trình phân hủy protein có hại và do đó loại bỏ chúng hoàn toàn.
Giáo sư Ciulli cho biết: "Chúng ta biết có nhiều protein hoạt tính gây ra bệnh ung thư nhưng chúng ta không thể ngăn chặn điều này xảy ra. Vấn đề chính là chúng ta không thể tìm thấy các phân tử nhỏ có thể liên kết thành công với các protein này và đồng thời cản trở chức năng của chúng.”
“Đây là một khu vực rất phức tạp. Các protein có thể tạo ra những điều chỉnh giả trong tế bào và cực kì khó khăn để ức chế. Nghiên cứu trong phòng thí nghiệm của chúng tôi trong vài năm gần đây đã góp phần thiết lập một cách tiếp cận khác. Phương pháp mới đã được lý thuyết hóa trong nhiều năm nhưng nhờ những nghiên gần đây chúng mới được công nhận một cách đầy đủ.”
“Thay vì sử dụng phân tử nhỏ để thử và vô hiệu hóa protein có hại, chúng tôi đã phát triển một phương pháp mới để sửa đổi. Cách này được sử dụng để thu hút các protein trung hòa, gắn kết chúng với những protein có hại và chống lại chúng. Từ đó bắt đầu một quá trình suy thoái ", giáo sư Ciulli cho biết thêm.
Giáo sư Ciulli và các đồng nghiệp đã tập trung sự chú ý vào một phân tử phân hủy hóa học gọi là PROTAC (Proteosysis-targeting chimer molecules).
Các nhà nghiên cứu đã tạo ra cấu trúc tinh thể X-quang đầu tiên của một PROTAC - liên kết với cả protein có hại và chất trung tính. Họ thấy rằng nó có thể được sử dụng như một nam châm để gắn hai protein mục tiêu lại với nhau.
Giáo sư Ciulli nói: "Khám phá này cung cấp những hiểu biết đầu tiên về cách thức hoạt động của PROTAC và làm thế nào chúng ta có thể phân hủy các protein mục tiêu một cách có chọn lọc?”
"Điều này thể hiện sự thay đổi mô hình trong việc can thiệp hóa học có chọn lọc đối với các protein. Những protein này gây ra bệnh tật nhưng cho đến nay chúng ta vẫn chưa thể tìm ra cách chữa trị. Nó giống như một thứ mà không thể chọc thủng được."
Công việc của nhóm Dundee là tập trung vào ghép nối một trong các protein bromodomain của BET là BRD4 - đây là một loại thuốc mục tiêu trong điều trị ung thư - với một loại BRD4 suy biến được gọi là MZ1.
Họ phát hiện ra rằng MZ1 có thể kéo hai protein lại với nhau bằng cách MZ1 tự gấp lại. Một khi hai protein này được kết hợp trong “nụ hôn” tương tác sẽ dẫn đến sự suy thoái mục tiêu.
Các protein tương tự BRD2 và BRD3 cũng không tương tác với các protein trung tính. Vì đó mà các nhà nghiên cứu có thể thiết kế những chất phân hủy mới mà không cần đến các protein này trong quá trình phân hủy.
Kết quả này rất quan trọng bởi vì nó giải thích cách những phân tử phân hủy có thể được thiết kế như thế nào trong tương lai? Và việc thiết kế đó là để giảm đến mức tối thiểu các tác động đi trệch mục tiêu, và không giống như việc sử dụng các chất ức chế thông thường.
Giáo sư Ciulli cho biết đã có những dấu hiệu đầy hứa hẹn từ ngành dược phẩm về việc đầu tư trong lĩnh vực nghiên cứu này.
"Bây giờ chúng ta đã hiểu rõ hơn cách chuyển chất ức chế thành chất phân hủy. Con đường để chuyển đổi chất phân hủy thành thuốc sẽ gặp rất nhiều khó khăn và chúng tôi không thể tự đi một mình được. Thật là thú vị khi nhìn thấy ngành dược phẩm đã có những cam kết nghiêm túc. Chúng ta có thể lạc quan vì điều này,” giáo sư Ciulli phát biểu.
Toàn bộ kết quả nghiên cứu đã được công bố trên tạp chí Nature Chemical Biology.