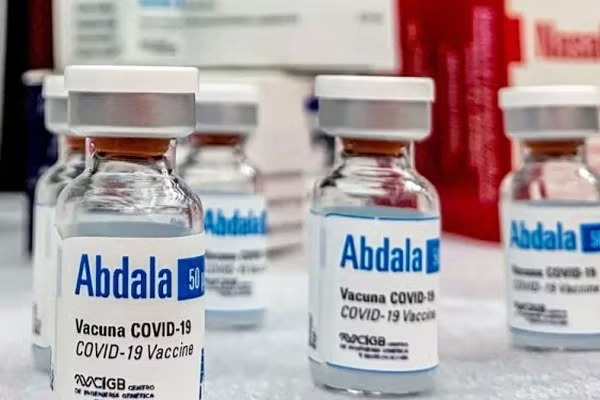
Vắc xin Abdala được sản xuất thành phẩm tại Công ty AICA Laboraries, Base Business Unit (BBU) AICA - Cuba và được xuất bán thành phẩm, đóng gói cấp 2 tại Trung tâm Kỹ thuật Di truyền và Công nghệ Sinh học (CIGB) - Cuba.
Vắc xin Abdala mỗi liều 0,5ml chứa 50 mcg Vắc xin protein tái tổ hợp chứa vùng liên kết với thụ thể (RBG) của vi-rút SARS-CoV-2, bào chế ở dạng hỗn dịch tiêm bắp. Vắc xin được đóng gói hộp 10 lọ, mỗi lọ chứa 10 liều, mỗi liều 0,5ml.
Bộ Y tế đã phê duyệt có điều kiện vắc xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 đối với loại vắc xin này vào ngày 17/9/2021.
Các trường hợp nên thận trọng khi tiêm vắc xin Abdala
Vắc xin này chỉ định tiêm phòng Covid-19 cho người từ 19-65 tuổi; gồm 3 liều, khoảng cách giữa các liều là 14 ngày; mỗi liều 0,5 ml, tiêm bắp.
Vắc xin Abdala chống chỉ định cho người dưới 19 tuổi, người mẫn cảm với bất cứ thành phần nào của vắc xin (bao gồm cả thiomersal).
Người mắc bệnh mạn tính, tự miễn dịch hoặc bệnh chuyển hóa nội tiết: Phải cân nhắc trước khi tiêm;
Người bệnh tăng huyết áp: Nên hoãn tiêm chủng cho đến khi kiểm soát được huyết áp.
Người đang bị nhiễm trùng cấp tính: Hoãn tiêm chủng vắc xin Abdala cho đến khi giải quyết hết được tình trạng nhiễm trùng.
Đối với phụ nữ có thai: Kinh nghiệm sử dụng vắc xin này ở phụ nữ có thai còn hạn chế. Các nghiên cứu trên động vật chứng minh vắc xin không ảnh hưởng trực tiếp hoặc gián tiếp đối với thai kỳ, sự phát triển của thai, đến bà mẹ trong khi sinh hoặc sau khi sinh.
Chỉ định tiêm vắc xin Abdala trong thai kỳ nên được xem xét nếu lợi ích lớn hơn các nguy cơ rủi ro tiềm ẩn đối với mẹ và thai nhi.
Về tiêm chủng đồng thời với các vắc xin khác, hướng dẫn của Bộ Y tế nêu rõ không có thông tin về sự tương tác của vắc xin phòng Covid-19 Abdala với các loại vắc xin khác.
Về phản ứng sau tiêm vắc xin Abdala
Các phản ứng sau tiêm thể nhẹ chiếm 97% phản ứng sau tiêm chủng và không phải điều trị bằng thuốc, thường xuất hiện từ 24 đến 48 giờ sau tiêm vắc xin.
Các tác dụng không mong muốn xảy ra cao hơn sau liều đầu tiên và giảm sau các liều tiếp theo.
Thử nghiệm lâm sàng sử dụng 215.267 liều cho thấy các biến cố bất lợi rất ít gặp, chỉ từ 0,1 đến 1% tổng số liều tiêm.
Chủ yếu phản ứng tại chỗ, hầu hết là đau tại chỗ tiêm, đỏ và cứng (0,85%).
Các phản ứng toàn thân: Nhức đầu (0,54%), tăng huyết áp (0,27%), buồn ngủ (0,18%) và mệt mỏi (0,14%).
Các phản ứng: Buồn nôn, nôn, đau khớp và tình trạng khó chịu chung xảy ra ít hơn (0,1%).
Qua sử dụng hơn 3 triệu liều trong cộng đồng, ghi nhận rất hiếm các trường hợp phản vệ, không có trường hợp tử vong hoặc các tác dụng phụ nghiêm trọng khác liên quan đến tiêm chủng.