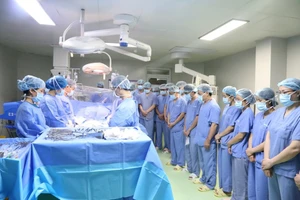
(GD&TĐ) - Cục Quản lý Dược Bộ Y tế vừa ban hành văn bản đình chỉ lưu hành và thu hồi thuốc điều trị bệnh đường hô hấp MIRACEF 50 OS (Cefpodoxime proxetil for oral suspension) do không đạt tiêu chuẩn chất lượng về chỉ tiêu định lượng.
 |
| Ảnh MH |
Thuốc MIRACEF 50 OS bị đình chỉ lưu hành trên toàn quốc và thu hồi thuộc lô số E037, Ngày SX: 06/2012, HD: 05/2015, SĐK:VN-14461-12, do công ty Miracle Labs (P) Ltd., India sản xuất, công ty Cổ phần Dược Thiết bị Y tế Đà Nẵng nhập khẩu.
Thuốc MIRACEF 50 OS không đạt tiêu chuẩn chất lượng về chỉ tiêu định lượng. Mẫu thuốc phát hiện không đạt tiêu chuẩn được lấy tại Công ty TNHH Thương mại Dược phẩm Trung Nghĩa (Quầy 115, tầng 1, HAPUMEDICENTER, số 1, Nguyễn Huy Tưởng, Thanh Xuân, Hà Nội).
Cục Quản lý Dược yêu cầu các cơ sở sản xuất phối hợp với nhà cung cấp phải khẩn trương thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn nói trên và báo cáo về Cục trước 20/3/2013.
Hải Hà